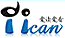原电池和电解池在高一化学《必修二》以及高二《化学反应原理》中均有相关介绍,但是这两个“池”子的结构及原理,有些同学混淆不清。下面对这两种装置进行对比分析。
图1(左) 图1(右)
上图中, 图1(左)侧装置的“池”为原电
池,Zn为负极,Pt为正极,电子从Zn电极流出,经过外电路,最终流向Pt电极, H+在Pt电极上得到电子,产生H2。所以,在原电池中,负极(上)失去电子,发生氧化反应;正极(上)得到电子,发生还原反应。要强调的是,原电池反应一定是一个自发的氧化还原反应,电极本身可以参加反应也可以不参加反应,但是两极上一定同时发生着氧化还原反应(负极氧化,正极还原)。
左图中, 图1(右)侧装置,即原电池的作用对象(外电路),也是一个“池”,这是一个电解池。与Zn电极(电源负极)相连的电极称为电解池的阴极,而与Pt电极(电源正极)相连的电极称为电解池的阳极。因为电子从Zn电极(电源负极) 流向阴极,所以阴极上发生还原反应(负极氧化,阴极还原);而电子又从阳极回到Pt电极(电源正极),所以阳极上发生氧化反应(阳极氧化,正极还原)。
图2中,将直流电源简略成一符号
“ ■ ■”,a 侧短竖线表示电源负极, b侧长竖线表示电源正极。那么与a相连的c电极为阴极,与b相连的d电极为阳极。可以很轻松地判断出电子方向:从a到c,再从d回到b;电流方向:从b到d,再从c回到a。a极(上)氧化,c极(上)还原;d极(上)氧化,b极(上)还原。 (市实高 王荣)
图2